上海金畔生物科技有限公司代理日本同仁化学 DOJINDO代理商全线产品,欢迎访问官网了解更多信息
C8H13N3O4
215.21
关联产品
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/0423c2d27b1d8f37c51dbedbf96451eca444ff9e.png)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/4a5bee0e3eaa552c6266de57bf3068864a50e57f.jpg)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/158d0d28fc8cf12cb751090accd89be6a6b6cd11.jpg)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/6a723d6b0f9a44b719e7ad1ebd636d510088d042.jpg)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/8c8e77ebf3db66c927e0c558d0d038cb47a18fb3.png)

上海金畔生物科技有限公司代理日本同仁化学 DOJINDO代理商全线产品,欢迎访问官网了解更多信息
C8H13N3O4
215.21
关联产品
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/0423c2d27b1d8f37c51dbedbf96451eca444ff9e.png)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/4a5bee0e3eaa552c6266de57bf3068864a50e57f.jpg)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/158d0d28fc8cf12cb751090accd89be6a6b6cd11.jpg)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/6a723d6b0f9a44b719e7ad1ebd636d510088d042.jpg)
![NOR 3试剂货号:N390 (±)-(E)-4-乙基-2-[(E)-羟基氨基]-5-硝基-3-己烯胺((±)-(E)-4-Ethyl-2-[(E)-hydroxyimino]-5-nitro-3-hexenamide) CAS号:138472-01-2](http://cn.jinpanbio.com/wp-content/uploads/2024/04/8c8e77ebf3db66c927e0c558d0d038cb47a18fb3.png)
上海金畔生物科技有限公司代理日本同仁化学 DOJINDO代理商全线产品,欢迎访问官网了解更多信息
NOR 3试剂 N390 NO供体
氧化应激与自由基
品名货号用途
| NOR 3试剂 | N390 | NO供体 |
| S-Nitrosoglutathione试剂 | N415 | NO供体 |
| Carboxy-PTIO试剂 | C348 | NO检测 |
| 2,3-Diaminonaphthalene(for NO detection)试剂 | D418 | NO研究 |
| DTCS Na试剂 | D465 | NO研究 |
细胞中的氧化应激是由代谢、电离辐射和与DNA直接相互作用的致癌化合物产生的ROS导致的。在代谢的过程中,小部分的氧由于一个电子的还原变成超氧阴离子,接着超氧阴离子被超氧化物岐化酶 (SOD) 转变成氧气和过氧化氢。过氧化氢由过氧化氢酶或谷胱甘肽过氧化物酶还原成水。然而如果过氧化氢并没有被这些酶完全还原,当它被铁(Fenton反应)氧化将产生反应性极强的羟自由基。羟自由基还可以由紫外线照射产生或直接电离辐射水产生。羟自由基可以与脂反应产生脂质过氧化物。然而并非所有ROS都是有害的。次氯酸盐离子是一种由中性粒细胞的髓过氧化物酶产生的过氧化氢衍生而来的ROS,它具有杀菌活性。NO也称为内皮来源的舒张因子,它是由NO合成酶产生的。不过NO和超氧阴离子反应可产生具有细胞毒性的过氧亚硝基阴离子。ROS和活性氮化合物在生物系统中具有许多不同的活性。相应地好氧生物会产生防止氧化应激的防御机制。最近在对防御机制以及氧化损伤与疾病或老化过程之间关系的研究中,氧化应激已成为许多研究的焦点。最终已发展出许多用于检测ROS相关或ROS来源的物质的方法,这些物质包括超氧阴离子、超氧化物岐化酶、谷胱甘肽、谷胱甘肽还原酶、谷胱甘肽过氧化物酶、DNA损伤、8-氧基鸟嘌呤、8-硝基鸟嘌呤和蛋白质羰基等。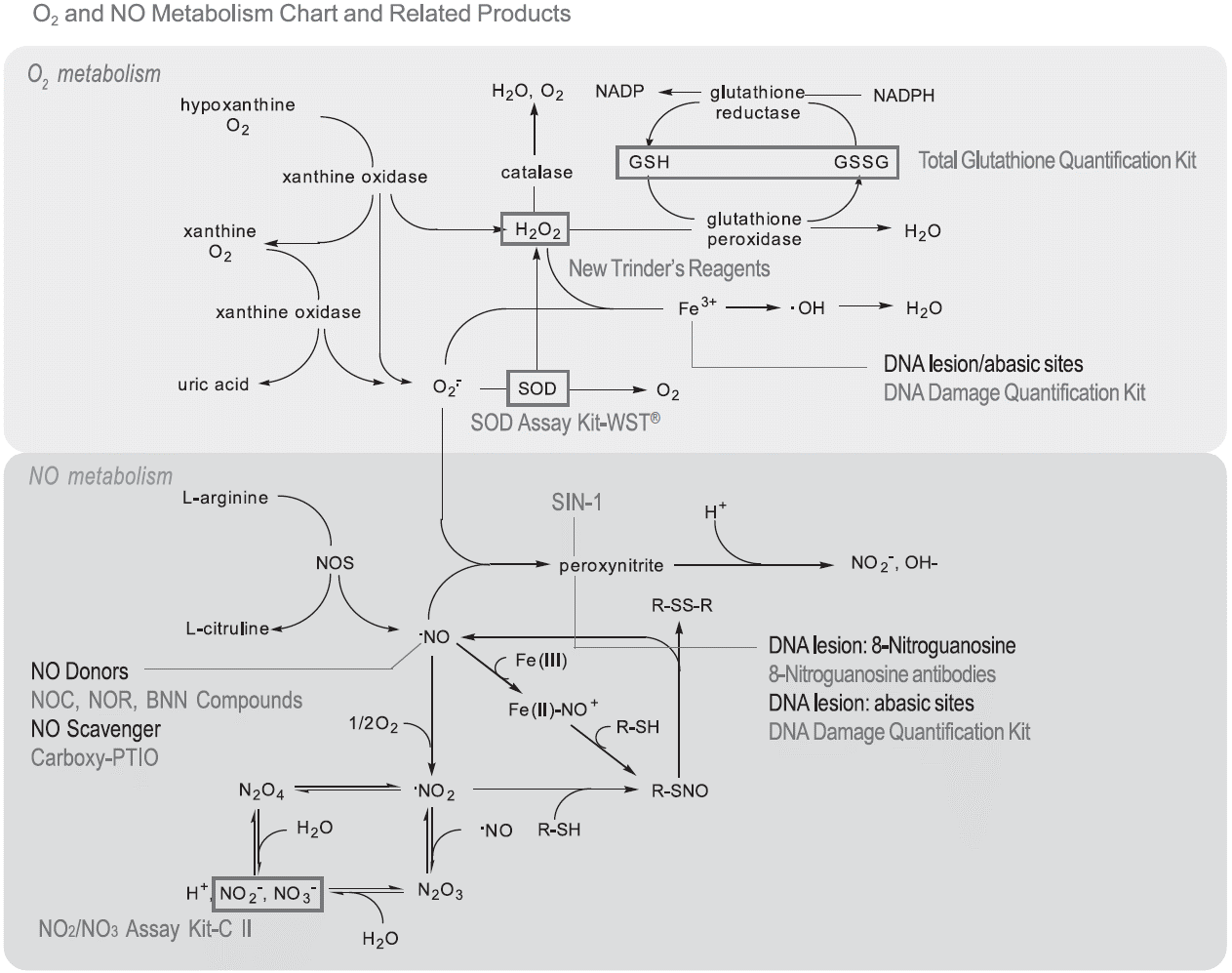
上海金畔生物科技有限公司代理日本同仁化学试剂盒全线产品,欢迎访问日本同仁化学dojindo官网了解更多信息。
 NOR 3
NOR 3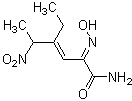
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 10 mg | ¥14,100 | 345-06941 |
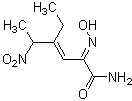

・本製品を粉末の状態で取り出し使用する場合、性状の性質上、静電気等の要因で容器内に付着し、取り出しにくい場合があります。
・容器内に付着し、取り出せなかった粉末に関しては、使用する溶媒を容器に入れ、溶かし出して使用してください。
1) Y. Kita, R. Ozaki, S. Sakai, T. Sugimoto, Y. Hirasawa, M. Ohtsuka, H. Senoh, K. Yoshida and K. Maeda, "Antianginal Effects of FK409, a New Spontaneous NO Releaser", Br. J. Pharmacol., 1994, 113, 1137.
2) Y. Kita, Y. Hirasawa, K. Yoshida and K. Maeda, "Antiplatelet Activities of FK409, a New Spontaneous NO Releaser", Br. J. Pharmacol., 1994, 113, 385.
3) M. Hino, M. Iwami, M. Okamoto, K. Yoshida, H. Haruta, M. Okuhara, J. Hosoda, M. Kohsaka, H. Aoki and H. Imanaka, "FK409, a Novel Vasodilator Isolated from the Acid-treated Fermentation Broth of Streptomyces Griseosporeus I. Taxonomy, Fermentation, Isolation, and Physico-chemical and Biological Characteristics", J. Antibiot., 1989 XLII(11), 1578.
4) S. Shibata, N. Satake, N. Sato, M. Matsuo, Y. Koibuchi and R. K. Hester, "Characteristics of the Vasorelaxing Action of (3E)-4-Ethyl-2-hydroxyimino-5-nitro-3-hexamide FK409, a New Vasodilator Isolated from Microbial Sources, in Isolated Rabbit Arteries", J. Cardiovasc. Pharmacol., 1991, 17(3), 508.
5) Y. Kita, Y. Hirasawa, K. Maeda, M. Nishio and K. Yoshida, "Spontaneous Nitric Oxide Release Accounts for the Potent Pharmacological Actions of FK409", Eur. J. Pharmacol., 1994, 257, 123.
6) J.-L. Decout, B. Roy, M. Fontecave, J.-C. Muller, P. H. Williams and D. Loyaux, "Decomposition of FK409, a New Vasodilator: Identification of Nitric Oxide as Metaborite", Bioorg. Med. Chem. Lett., 1995, 5(9), 973.
7) S. Fukuyama, Y. Kita, Y. Hirasawa, T. Azuma, A. Sato, N. Morokoshi, S. Koda, T. Yasuda, S. Oka and H. Sakurai, "A New Nitric Oxide (NO) Releaser: Spontaneous NO Release from FK409", Free Rad. Res., 1995, 23(5), 443.
8) Y. Kita, K. Ohkubo, Y. Hirasawa, Y. Katayama, M. Ohno, S. Nishino, M. Kato and K. Yoshida, "FR144420, a Novel, Slow, Nitric Oxide-releasing Agent", Eur. J. Pharmacol., 1995, 275, 125.
9) M. Kato, S. Nishino, M. Ohno, S. Fukuyama, Y. Kita, Y. Hirasawa, I. Nakanishi, H. Takasugi and K. Sakane, "New Reagents for Controlled Release of Nitric Oxide. Structure-stability Relationships", Bioorg. Med. Chem. Lett., 1996, 6(1), 33.
10) Y. Kita, Y. Hirasawa, S. Fukuyama and K. Yoshida, "FK409, a Novel Spontaneous NO Releaser: Comparative Pharmacological Studies with ISDN", Cardiovasc. Rrug. Revi., 1996, 14(2), 148.
11) Y. Hirasawa, T. Sugimoto, S. Fukuyama, Y. Kato, H. Takamatu, M. Ohno, S. Nishino, M. Kato, K. Maeda, J. Seki and Y. Kita, "Antianginal Effects of FR144420, a Novel Nitric Oxide-releasing Agent", Eur. J. Pharmacol., 1996, 303, 55.
12) M. Sato and M. Kawatani, "Nitric Oxide Raises Cytosolic Concentrations of Ca2+ in Cultured Nodose Ganglion Neurons from Rabbits", Neurosci. Lett., 1996, 206, 69.
13) Y. Kita, Y. Hirasawa, S. Fukuyama, K. Ohkubo, Y. Kato, H. Takamatsu, M. Ohno, S. Nishino, M. Kato and J. Seki, "Oral Biological Activities of Spontaneous Nitric Oxide Releaser are Accounted for by their Nitric Oxide-releaseing Rates and Oral Absorption Manners", J. Pharmacol. Exp. Ther., 1996, 276(2), 421.
14) S. Fukuyama, Y. Hirasawa, Y. Kato, M. Nishino, M. Ohno, S. Nishino, K. Maeda, M. Kato and Y. Kita, "Structure-activity Relationships of Spontaneous Nitric Oxide Releasers, FK409 and its Derivatives", J. Pharmacol. Exp. Ther., 1997, 282(1), 236.
15) Y. Kita, Y. Hirasawa, Y. Kato, K. Ohkubo, M. Ohno, S. Nishino, M. Kato and S. Fukuyama, "Comparison of Hemodynamic Effects of Nitric Oxide (NO) Donors with Different NO-releasing Properties in Rats", J. Cardiovasc. Pharmacol., 1997, 30(2), 223.
16) Y. Hirasawa, Y. Kato, S. Fukuyama, M. Ohno, S. Nishino, M. Kato and Y. Kita, "Comparison of Antiplatelet Effect of two Nitric Oxide-donating Agents, FR146801 and FK409", Thrombosis Haemost., 1998, 79, 620.
NOCとNORは両方ともNO発生剤として使用されますが、どう違うのですか?
構造的には全く異なるタイプのNOドナーです。
性能の違いとしては
【NOC】
高水溶性
水溶液での調製が容易(NaOH溶液)
NOCは高pH(アルカリ性)ほどNO放出が遅くなる。
半減期は(37℃、pH7.4)
NOC7(5min) > NOC5(25min) > NOC12(100min) > NOC18(21hrs)
【NOR】
比較的水溶性が低い
有機溶媒(DMSO)溶液の方が安定に扱える。
経口投与が可能である。
NORは低pH(酸性)ほどNO放出が遅くなる。
半減期は(37℃、pH7.4)
NOR1(1.8min) > NOR3(30min) > NOR4(60min) > NOR5(20hrs)
NOR類を使用する際の溶解する溶媒は何がいいでしょうか?
乾燥DMSOをお使いください。
乾燥DMSOに溶解してストック溶液とし、所定量を試料溶液に加えます。
ストック溶液とした場合、一両日中にご使用下さい。
NO発生は事実上中性バッファー(サンプル溶液)に添加された時点から開始されます。
生理食塩水などの緩衝作用のないものでは、NOはきれいに放出しませんのでご注意ください。
NOR3の溶解性を教えてください。
NORs、NOCsの溶解性は以下の通りです。

*注意*
NORsは水にも溶けますが、ストック液の調整は「DMSO」で行ってください。
中性の水では溶解直後から分解(NOの放出)が始まります。


| 性状: | 本品は白色結晶性粉末で、ジメチルスルホキシドに溶ける。 |
|---|---|
| 純度(HPLC): | 98.0% 以上 |
| ジメチルスルホキシド溶状: | 試験適合 |
| 保存条件: 冷凍 |
